|
|
某些不含有Rox?均一化参比染料,或是无法在整个实验过程中使用参比染料的定量PCR平台,常常试图贬低使用参比染料的价值。然而事实是,在定量PCR反应过程中Rox?染料是一种非常有价值的工具,能带来以下多方面好处:
# |4 d( x. b$ U5 r- N[li]校正单次反应运行中由于泡沫或蒸发/冷凝而导致的信号改变;6 m6 \ t4 X- t) X7 t) w' D& j. }- F
[/li][li]为故障分析提供一项强有力的诊断工具:每次循环采集参比染料信号,不受PCR反应影响;3 }. g" a' I$ q" M5 b* d' @
[/li][li]均一化校正由于移液误差或蒸发所导致的批内体积差异;3 [5 i! g: {* U$ H" n# h! g# c
[/li][li]均一化校正批间体积差异,提供更连续一致的批间重复Ct值。
5 m' r, X: D/ w1 o[/li] 2 S; O: f' S+ V5 t* ]5 R$ N$ A
美国应用生物系统公司(Applied Biosystems)认识到均一化工具(Rox?参比染料)的好处,并在所有AB定量PCR仪上优化,以便实验人员充分利用Rox?参比染料所带来的好处。此外,所有AB生产的Real-Time PCR Master Mix试剂液都预掺入最合适量的Rox?参比染料,从而确保每次实验每个反应都获得最好的结果。3 D7 ], q! d) {! A$ r3 i# J
' _2 U7 W7 Z( _/ J b \
Rox?校正单次反应运行中的信号改变% {, a5 V6 O& ?; K
2 w; i7 I3 ^4 d8 O- Q% y! ?1 I
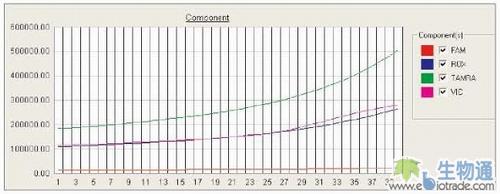
在理想反应条件下,报告荧光染料的信号值起始于基线,当反应体系中存在合适的靶分子时,报告荧光染料会随着PCR反应的进行,产生出一条典型的扩增曲线,仪器软件通过扩增曲线计算结果。如果扩增曲线只是简单地根据报告染料的荧光信号而绘制,将会难以区分样品的真实差异和随机反应条件带来的人为差异。现实中,有许多事件可能影响报告荧光染料的表现:泡沫会形成荧光信号尖峰;蒸发或冷凝会造成反应体系浓度改变,导致不同反应批次间荧光信号值增强或减弱(见图1)。这类事件会同时影响报告荧光染料和Rox?参比染料,所以使用AB的定量试剂与仪器时,根据Rn值绘制扩增曲线,采集的是报告荧光染料减去Rox?参比染料的荧光差值,任何潜在的人为误差因素都被均一化,从而排除在最终结果之外。
* B: \9 K, i1 a) Q H4 N) i# Q+ ?! [) T, M: P* T1 T
 , Y, O8 K; u+ P4 a. m! b , Y, O8 K; u+ P4 a. m! b
图1:多组分图显示Rox?信号和报告染料信号一同抬起,结果指示存在蒸发
% P5 L3 p0 ~( l/ ]
6 [: w4 O8 d/ B# A+ JRox?提供强大的故障分析工具
" M' ]9 O# s; w. c& \8 ?1 {' P5 ?1 G
Rox?参比染料作为故障分析工具的价值同样不应被低估。如果一个反应失败了,依靠Rox?参比染料确保在反应过程中有持续不变的信号标准十分重要。Rox?信号可以提供反应设置的信息提示:无Rox?信号,很明确地表明没有放置Master Mix试剂;异常大的信号值强度差异,提示可能放置了2倍反应体系;Rox?信号不规则变化,提示可能存在仪器故障。AB公司的技术支持在故障排除工作中总会使用Rox?参比染料,以帮助在更短时间内获得更多信息量的检测结果。' D+ `4 d# f4 J# B) x# y8 `) g
+ l5 M- J0 G( K- L
Rox?均一化反应体积差异" n7 i% _* g! @+ j
& F2 S" e0 ?! k6 _6 t/ r* J' ^* u. H: Y以下实验数据证明了Rox?参比染料在校正移液误差所导致的反应间均方差上的价值,同时也证明AB定量PCR仪器在使用或不使用Rox?参比染料都能获得很好的性能表现和精确性。2 n" `7 {1 l/ U _7 z( |3 D2 ?
实验一:获得高精确性不一定需要Rox?
) e! ~7 ]9 n h/ G' l y8 H8 Y从AB RNase P Instrument verification Plate中取出反应混合液,分别移液入对应的Fast 96孔板中。在AB 7500 Fast Real-Time PCR仪上运行这块板。数据分析分别采用2组模式,一组为正常的减去Rox?参比染料,另一组将参比染料设置成“None”,从而显示使用Rox?信号均一化处理数据的价值。技术重复(24次重复)的结果显示,使用Rox?和不使用Rox?都得到了很好的结果。使用Rox? 一组的Ct值SD(标准偏差)0.042,不使用Rox? 一组的Ct值SD(标准偏差)0.108(见图2)。
$ Q! K+ J& k) A* s T- {) b
1 C9 P, C2 q1 L7 o. G: | `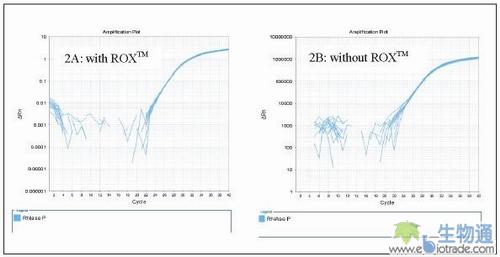
. P# J' j: l6 D9 w* K' c! c- [图2:技术重复的扩增曲线,分别采用Rox?校正(2A)和不采用Rox?校正(2B),显示重复的结果聚合紧密,散布很小。
. X' t. Q8 V \5 x a
$ {, P- g/ D# i) a/ M# ?实验二:Rox?均一化处理校正移液错误- k* v1 p# o+ n
通过系统地减少从RNase P Plate中移出的样品,加入分子纯级水补齐体系,来模拟移液错误对运行精确性的影响。图2描绘了实验一中的原体积样本,以及3个移液错误重复:分别含0.5, 1.0 和1.5μl of ddH2O(样本体积相应减少)。数据分析时使用Rox?参比染料校正初始浓度差异(由移液错误导致的),得到的Ct值SD(标准偏差)为0.075;而不使用Rox?参比染料校正的Ct值SD(标准偏差)为0.174(见图3)。
% M P) q0 F% p5 |5 B' z# i- @" a: P6 \0 v" z8 Y/ Q4 E' w
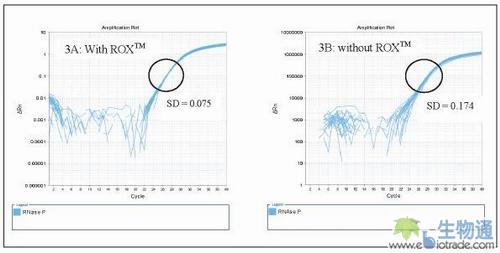
- z' H5 i0 f3 F/ S9 }/ G图3:技术重复与3重模拟样本移液错误(分别用0.5, 1.0 和 1.5μl ddH2O替代等量样本模板)的扩增曲线。使用Rox? 可以校正起样本始体积(或浓度)的轻微差异(3A),而不使用Rox?时可以明显看到轻微的散布(3B)。) ?1 v( w( O; i# B" M- G8 @& K9 ?+ e
% u. _& [) [+ w% j4 F
实验三:Rox?均一化处理确保定量反应精确性
w7 t/ q* w f J0 o相似地,直接从RNAse P Plate中移出反应混合液进行重复实验绘制标准曲线,比较使用Rox?和不使用Rox?分析时的精确性差异(见图4),结果R2值分别是0.997 和 0.99。( W0 p$ _/ g }& U
; Y: @0 Z- ^; }2 A- ^
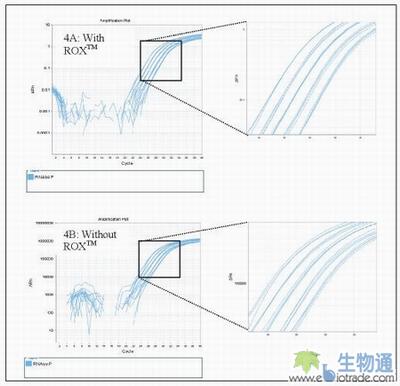
+ l0 E( |' s3 k5 \# n图4:重复RNAse P标准品的扩增曲线,数据分析时分别用Rox?(4A)和不用Rox?(4B),结果表现都很好。% K( G! g. h+ ~' m
b# ?; A2 A( q+ D
当反应体系中部分样品被1μl ddH2O替代,Rox?均一化处理能够校正此类小错误,而当分析不包含Rox?参比染料校正时,各个标准组中很明显地出现了更大的点散布(见图5和表1)。6 Q: B+ {7 q9 m" J# e
4 z+ U: u; a) ?" r$ o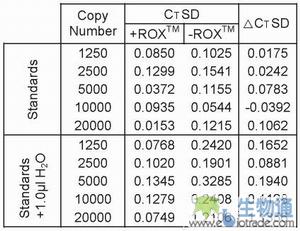 + M" K5 L6 W- O* c+ \ + M" K5 L6 W- O* c+ \
表1:计算重复进行RNAse P标准曲线实验的标准偏差(SD),将其与1μl反应混合液被ddH2O取代的实验结果比较。使用Rox?校正可有效减少错误。
" |0 L0 {* _7 n* w( K8 _1 t0 m! Q
* x- W* c$ r/ ^ `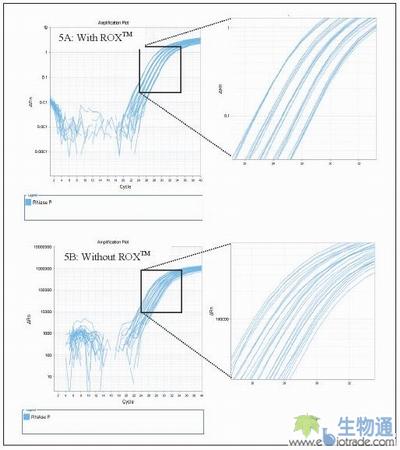
1 ]7 ]9 i; D3 h+ a# }图5:重复RNAse P标准品,及模拟移液错误样本(1μl反应混合液被ddH2O取代),绘制扩增曲线。数据分析时分别使用Rox?(5A)和不用Rox?(5B),证明Rox?可以校正由轻微起始样本浓度或反应体积错误而造成的差异。
, S) p# {9 b9 t) V( G9 Q3 J' E/ X4 j' X3 g
表1显示了各个浓度重复反应的结果标准偏差(SD)。其中,直接从RNAse P plate中移出反应混合液进行的重复实验,使用Rox?或不使用Rox?所得的Ct值SD(标准偏差)差异很小(平均小于0.04)。可是当模拟移液错误时,不使用Rox?校正所得的Ct值SD差异远远大于使用Rox?校正时的结果(10倍于后者)。以上结果再次证明了使用Rox?参比染料分析Real-Time PCR实验数据时的优势。% z: v) ]7 \* o. u! P' ]
' T& O' H* S% K2 z/ `总之,以上实验的模拟错误只是任何实验室Real-Time PCR平台在实际操作中可能遇到的诸多错误中的一个。考虑到这类错误在日常中常常会出现,再加上上文中提到的其它与定量PCR平台相关的可能人为错误,显而易见,分析Real-Time PCR数据时使用Rox?均一化具有明显的好处。 |
本帖子中包含更多资源
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
|